Структурная формула
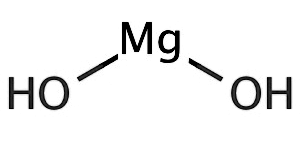 |
Истинная, эмпирическая, или брутто-формула: H2MgO2
Химический состав Гидроксида магния
| Символ | Элемент | Атомный вес | Число атомов | Процент массы |
|---|---|---|---|---|
| H | Водород | 1,008 | 2 | 3,5% |
| Mg | Магний | 24,312 | 1 | 41,7% |
| О | Кислород | 15.999 | 2 | 54,9% |
Молекулярная масса: 58,326
Гидроксид магния — неорганическое вещество, осно́вный гидроксид металла магния. Слабое нерастворимое основание.
Описание
При стандартных условиях гидроксид магния представляет собой бесцветные кристаллы с гексагональной решёткой. При температуре выше 350 °C разлагается на оксид магния и воду. Поглощает углекислый газ и воду из воздуха с образованием основного карбоната магния. Гидроксид магния практически нерастворим в воде, но растворим в солях аммония. Является слабым основанием. Встречается в природе в виде минерала брусита.
Получение
- Взаимодействие растворимых солей магния с щелочами.
- Взаимодействие раствора хлорида магния с обожжённым доломитом.
- Взаимодействие металлического магния с парами воды.
Химические свойства
- Как и все слабые основания, гидроксид магния термически неустойчив. Разлагается при нагревании до 350 °C.
- Взаимодействует с кислотами с образованием соли и воды (реакция нейтрализации).
- Взаимодействие с кислотными оксидами с образованием соли и воды.
- Взаимодействие с горячими концентрированными растворами щелочей с образованием гидроксомагнезатов.
Применение
Гидроксид магния применяется для связывания диоксида серы, как флокулянт для очистки сточных вод, в качестве огнезащитного средства в термопластических полимерах (полиолефины, ПВХ), как добавка в моющие средства, для получения оксида магния, рафинирования сахара, в качестве компонента зубных паст. В медицине его применяют в качестве лекарства для нейтрализации кислоты в желудке, а также как очень сильное слабительное. В Европейском союзе гидроксид магния зарегистрирован в качестве пищевой добавки E528.
