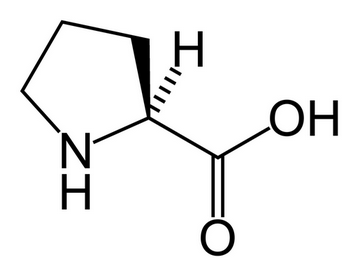
Структурная формула
 |
 |
Истинная, эмпирическая, или брутто-формула: C5H9NO2
Химический состав Пролина
| Символ | Элемент | Атомный вес | Число атомов | Процент массы |
|---|---|---|---|---|
| C | Углерод | 12,011 | 5 | 52,2% |
| H | Водород | 1.008 | 9 | 7,9% |
| N | Азот | 14,007 | 1 | 12,2% |
| O | Кислород | 14,007 | 2 | 27,8% |
Молекулярная масса: 115,132
Пролин (пирролидин-α-карбоновая кислота) — гетероциклическая аминокислота, в которую атом азота входит в составе вторичного, а не первичного, амина (в связи с чем пролин часто неправильно называют иминокислотой). Существует в двух оптически изомерных формах — L и D, а также в виде рацемата. L-пролин — одна из двадцати двух протеиногенных аминокислот (помимо 20 широко известных выделяют пирролизин и селеноцистеин). Считается, что пролин входит в состав белков всех организмов. Особенно богат пролином основной белок соединительной ткани — коллаген. В составе белков атом азота пролина не связан с атомом водорода, таким образом, пептидная группировка X-Pro не может быть донором водорода при формировании водородной связи. Обладая конформационно жесткой структурой, пролин очень резко изгибает пептидную цепь. Участки белков с высоким содержанием пролина часто формируют вторичную структуру полипролиновой спирали II типа. Представляет собой бесцветные легко растворимые в воде кристаллы, плавящиеся при температуре около 220 °C. Также хорошо растворим в этаноле, хуже — в ацетоне и бензоле, не растворим в эфире. В организме пролин синтезируется из глутаминовой кислоты. Пролин, как и гидроксипролин, в отличие от других аминокислот, не образует с нингидрином пурпура Руэмана, а дает жёлтое окрашивание. В составе коллагена пролин при участии аскорбиновой кислоты окисляется в гидроксипролин. Чередующиеся остатки пролина и гидроксипролина способствуют созданию стабильной трёхспиральной структуры коллагена, придающей молекуле прочность.
