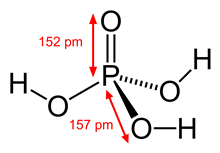
Структурная формула
 |
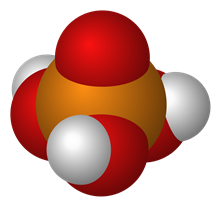 |
Истинная, эмпирическая, или брутто-формула: H3O4P
Химический состав Ортофосфорной кислоты
| Символ | Элемент | Атомный вес | Число атомов | Процент массы |
|---|---|---|---|---|
| H | Водород | 1,008 | 3 | 3.1% |
| O | Кислород | 15.999 | 4 | 65.3% |
| P | Фосфор | 30.974 | 1 | 31.6% |
Молекулярная масса: 97,994
Ортофо́сфорная кислота́(фо́сфорная кислота́) — неорганическая кислота средней силы, с химической формулой H3PO4, которая при стандартных условиях представляет собой бесцветные гигроскопичные кристаллы. При температуре выше +213 °C она превращается в пирофосфорную кислоту H4P2O7. Очень хорошо растворима в воде. Обычно ортофосфорной (или просто фосфорной) кислотой называют 85 %-й водный раствор (бесцветная сиропообразная жидкость без запаха). Растворима также в этаноле и других растворителях.
Получение
Фосфорную кислоту получают из фосфата:
Ca3(PO4)2 + 3H2SO4 → 3CaSO4 + 2H3PO4
Можно получить гидролизом пентахлорида фосфора:
PCl5 + 4H2O → H3PO4 + 5HCl
Или взаимодействием с водой оксида фосфора(V), полученного сжиганием фосфора в кислороде:
P2O5 + 3H2O → 2H3PO4
С водой реакция идет очень бурно, поэтому оксид фосфора(V) обрабатывают нагретым до 200 °C концентрированным раствором ортофосфорной кислоты.
Расплавленная ортофосфорная кислота и её концентрированные растворы обладают большой вязкостью, что обусловлено образованием межмолекулярных водородных связей.
Свойства
H3PO4 — трёхосновная кислота средней силы. При взаимодействии с очень сильной кислотой, например, с хлорной HClO4, фосфорная кислота проявляет признаки амфотерности — образуются соли фосфорила, например [Р(ОН)4]ClO4.
В водных растворах подвергается электролитической диссоциации в три стадии с образованием катиона гидроксония. Степень диссоциации и вид зависят от pH раствора:
H3PO4(aq) + H2O(l) ↔ H3(aq)O+ + H2PO4(aq)- Ks1 = 6,9 * 10-3
H2PO4(aq)- + H2O(l) ↔ H3O+ + HPO4(aq)2- Ks2 = 6,2 * 10-8
HPO4(aq)2- + H2O(l) ↔ H3(aq)+ + PO4(aq)3- Ks3 = 4,7 * 10-13
Отличительной реакцией ортофосфорной кислоты от других фосфорных кислот является реакция с нитратом серебра, при этом образуется жёлтый осадок:
H3PO4 + 3AgNO3 → Ag3PO4 + 3HNO3
Качественной реакцией на ион H2РО4− является образование ярко-жёлтого осадка молибденофосфата аммония:
H3PO4 + 12[NH4]2MoO4 + 21HNO3 → [NH4]3PMo12O40 * 6H2O + 21NH4NO3 + 6H2O
Фосфаты
Соли фосфорной кислоты называются фосфатами. Фосфорная кислота образует одно-, двух- и трехзамещенные соли.
H3PO4 + NaOH → NaH2PO4 + H2O (дигидрофосфат натрия)
H3PO4 + 2NaOH → Na2HPO4 + 2H2O (гидрофосфат натрия)
H3PO4 + 3NaOH → Na3PO4 + 3H2O (фосфат натрия)
Дигидрофосфаты (однозамещенные фосфаты) имеют кислую реакцию, гидрофосфаты (двузамещенные фосфаты) — слабощелочную, средние (трехзамещенные фосфаты, или просто фосфаты) — щелочную.
Дигидрофосфаты обычно хорошо растворимы в воде, почти все гидрофосфаты и фосфаты растворимы мало. Прокаливание солей приводит к следующим превращениям:
NaH2PO4 → NaPO3 + H2O
2Na2HPO4 → Na4P2O7 + H2O
Фосфаты при прокаливании не разлагаются, исключение составляет фосфат аммония (NH4)3PO4.
Органические фосфаты играют очень важную роль в биологических процессах. Фосфаты сахаров участвуют в фотосинтезе. Нуклеиновые кислоты также содержат остаток фосфорной кислоты.
Применение
Используется при пайке в качестве флюса (по окисленной меди, по чёрному металлу, по нержавеющей стали), для исследований в области молекулярной биологии. Применяется также для очищения от ржавчины металлических поверхностей. Образует на обработанной поверхности защитную плёнку, предотвращая дальнейшую коррозию. Также применяется в составе фреонов, в промышленных морозильных установках как связующее вещество.
Авиационная промышленность
В составе гидрожидкостей НГЖ-5У и её иностранных аналогов.
Пищевая промышленность
Ортофосфорная кислота зарегистрирована в качестве пищевой добавки E338. Применяется как регулятор кислотности в газированных напитках, например в Кока-Коле.
Сельское хозяйство
В звероводстве (в частности, при выращивании норок) используют выпойку раствора ортофосфорной кислоты для профилактики повышенного рН желудка и мочекаменной болезни.
Стоматология
Ортофосфорная кислота применяется для протравливания (снятия смазанного слоя) эмали и дентина перед пломбированием зубов. При применении адгезивных материалов 2 и 3 поколения требуется протравливание эмали зуба кислотой, с последующим промыванием и просушиванием. Кроме дополнительных временных затрат на проведение, данные этапы несут в себе опасность возникновения различных ошибок и осложнений.
При нанесении ортофосфорной кислоты сложно проконтролировать степень и глубину деминерализации дентина и эмали. Это приводит к тому, что нанесенный адгезив не полностью (по всей глубине) заполняет открытые дентинные канальцы, а это в свою очередь не обеспечивает образование полноценного гибридного слоя.
Кроме того, не всегда удается полностью удалить ортофосфорную кислоту после её нанесения на дентин. Это зависит от того, каким способом сгущена фосфорная кислота. Остатки ортофосфорной кислоты ухудшают прочность бондинга, а также приводят к образованию так называемой «кислотной мины».
С появлением адгезивных материалов 4 и 5 поколения стали использовать технику тотального протравливания (дентин — эмаль). В адгезивных системах 6 и 7 поколения отдельный этап протравливания кислотой отсутствует, так как адгезивы являются самопротравливающимися. Хотя некоторые производители все же рекомендуют для усиления адгезии кратковременно протравливать эмаль и при использовании самопротравливащих адгезивов.
