Структурная формула
 |
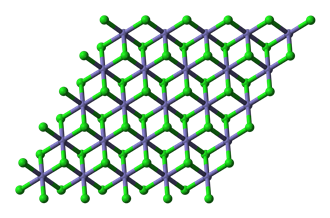 |
Истинная, эмпирическая, или брутто-формула: Cl2Fe
Химический состав Хлорида железа (ll)
| Символ | Элемент | Атомный вес | Число атомов | Процент массы |
|---|---|---|---|---|
| Cl | Хлор | 35,453 | 2 | 55,9% |
| Fe | Железо | 55,849 | 1 | 44,1% |
Молекулярная масса: 126,755
Хлорид железа (ll), хлористое железо Cl2Fe — средняя соль двухвалентного железа и соляной кислоты.
Свойства
Бесцветные кристаллы плотностью 1,93 г/см3, желтеющие на воздухе. Плавится при 677 °C, кипит — при 1026 °C. Хорошо растворим в воде, этаноле, ацетоне. Не растворяется в диэтиловом эфире. При растворении в воде слабо гидролизуется. Из водных растворов при температуре ниже 12,3 °C выкристаллизовывается FeCl2·6H2O; от 12,3 °C до 76,5 °C — FeCl2·4H2O; выше 76,5 °C — FeCl2·2H2O, переходящий при температурах более 120 °C в FeCl2·H2O. Проявляет восстановительные свойства: 2FeCl2 + Cl2 → 2FeCl3
Получение
Получают растворением железа в соляной кислоте (в частности, при травлении стальных изделий).
Fe
+ 2HCl → FeCl2 + H2O
FeO + 2HCl → FeCl2 + H2O
Fe(OH)2 + 2HCl → FeCl2 + 2H2O
2FeCl3 + SO2 + H2O → 2FeCl2 + H2SO4 + 2HCl
2FeCl3 + Fe → 3FeCl2
2FeCl3 + 2KI → 2FeCl2 + 2KCl + I2
2FeCl3 + H2 → 2FeCl2 + 2HCl
2FeCl3 + H2S → 2FeCl2 + S + 2HCl
Применение
Хлорид железа(II) применяют для получения хлорида железа(III). Также применяется в ювелирном деле. В медицине используется в качестве лекарственного средства для лечения и профилактики железодефицитной анемии. В России зарегистрирован под торговой маркой «Гемофер».
